Los hidrocarburos aromáticos corresponden a uno de las tres clases de compuestos orgánicos que podemos encontrar formando parte del petróleo, aunque estos se encuentran en menor proporción que los hidrocarburos alifáticos y cíclicos, pero estos compuestos también han adquirido gran importancia industrial. El termino aromático les fue conferido hace mucho tiempo, por el simple hecho de que algunos de ellos desprenden olores agradables.
Estos compuestos, en su mayoría, tienen como base la estructura del benceno, como sabrán, el benceno (C6H6) contiene un anillo plano con seis átomos de combinados con hidrógenos mediante enlaces simples y dobles. El anillo de benceno generalmente se representa como en la siguiente figura.

En la primera estructura, las líneas representan enlaces C-C, en esta también es común omitir los átomos de carbono e hidrógeno, expresándose únicamente con el hexágono y el circulo interno. El anillo de benceno es muy estable y sobrevive sin cambios en la mayoría de las reacciones químicas. Es muy diferente en reactividad y forma de los anillos fruncidos de seis miembros que se encuentran en los cicloalcanos.
Suelen encontrarse en mayor proporción en el carbón, más que en el petróleo, y además de su presencia en los combustibles, son utilizados en colorantes, plásticos, insecticidas, detergentes, solventes y muchos otros productos.

Estructura
Comenzamos con el más simple de estos compuestos, el benceno (C6H6) es de gran importancia comercial. La fórmula C6H6 parece indicar que el benceno tiene un alto grado de insaturación. (El hexano, el hidrocarburo saturado con seis átomos de carbono tiene la fórmula C6H14, ocho átomos de hidrógeno más que el benceno), cada átomo de carbono comparte un electrón con un átomo de hidrógeno y un electrón con cada átomo de carbono vecino. Entonces, para que una molécula sea considerada como un hidrocarburo arómatico debe obedecer algunas normas, entre las que se pueden mencionar:
- Debe ser cíclica, debe formar un anillo, lo que permite la existencia de estructuras resonantes.
- Debe ser plana (cada uno de los átomos que forman parte del anillo deben poseer hibridación sp2).
- Como tienen enlaces simples y dobles alternados, una molécula de estos compuestos debe ser capaz de deslocalizar sus electrones, por lo que se representan mediante un círculo dentro del anillo.
- Deben cumplir con la regla de Hückel; si al contar los electrones π este número es igual a 4n+2 son considerados aromáticos.
Los anillos de benceno pueden unirse (fusionarse) para dar compuestos aromáticos policíclicos más grandes. Siempre que cumplan las premisas descritas, son considerados compuestos aromáticos. Por ejemplo en las siguientes imágenes:

Nomenclatura
En el sistema de la Unión Internacional de Química Pura y Aplicada (IUPAC), los hidrocarburos aromáticos se denominan como derivados del benceno.En la siguiente figura se muestran algunos ejemplos.

Cuando se tiene solo un sustituyente en estas estructuras, es irrelevante si el sustituyente simple está escrito en la parte superior, lateral o inferior del anillo: un hexágono es simétrico y, por lo tanto, todas las posiciones son equivalentes. Pero cuando hay más de un sustituyente, las esquinas del hexágono ya no son equivalentes, por lo que debemos designar las posiciones relativas. Hay tres posibles bencenos disustituidos, y podemos usar números para distinguirlos.

Aunque algunos compuestos se nombran exclusivamente por las reglas de la IUPAC, algunos se conocen con mayor frecuencia por nombres comunes, como los siguientes:
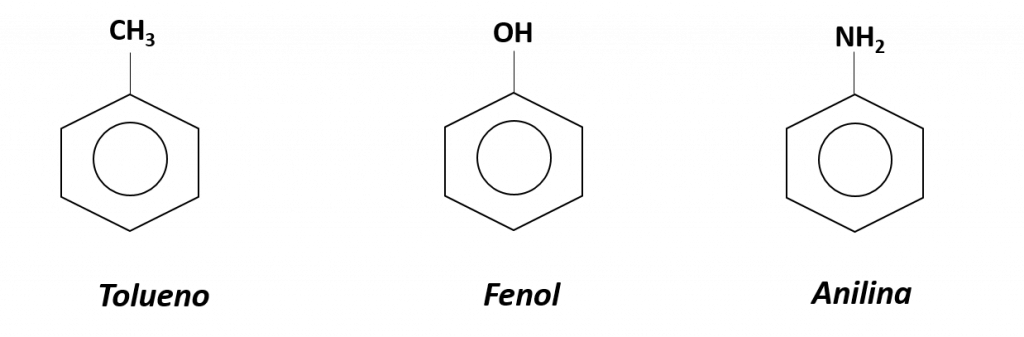
También se usan nombres comunes: el prefijo orto (o-) para la disustitución 1,2, meta (m-) para la disustitución 1,3 y para (p-) para la disustitución 1,4. Los nombres de los sustituyentes se enumeran en orden alfabético. El primer sustituyente recibe el número más bajo. Cuando se usa un nombre común, el átomo de carbono que lleva el grupo responsable del nombre recibe el número 1.

Referencias:
Morrison, R. T. y Boyd, R. N. (1990). Química Orgánica Quinta Edición. Editorial Addison-Wesley Iberoamericana.
Chemistry Libre Texts. Aromatics Hidrocarbons.
Wikipedia.com. Hidrocarburos aromáticos.
Posted from my blog with SteemPress : https://moronej.000webhostapp.com/2020/03/hidrocarburos-aromaticos-estructura-y-propiedades
