Hola estimados amigos de la comunidad científica de Hive!
Entre ellas se encuentran la disminución de la presión de vapor del disolvente, el aumento del punto de ebullición, el descenso del punto de congelación y la presión osmótica.
Revisemos detalladamente el aumento del punto de ebullición, ¡les invito a leer!
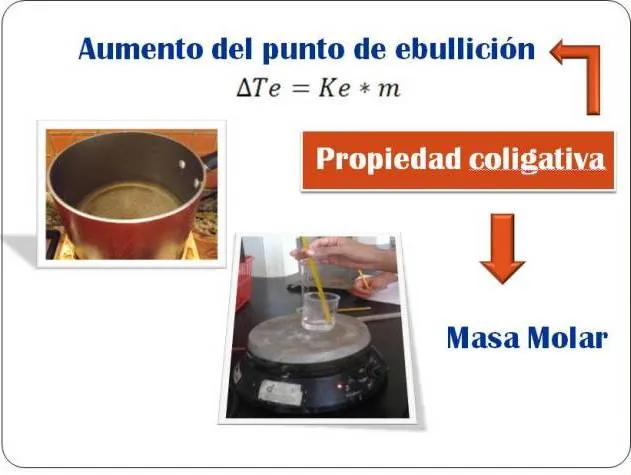
Aumento del punto de ebullición
Comencemos por definir punto de ebullición, como la temperatura a la cual la presión de vapor de un líquido es exactamente igual a la presión de vapor aplicada. Si nos referimos a punto de ebullición normal, es la temperatura a la cual la presión de vapor de un líquido es exactamente igual a la presión de 1 atm (760 torr). La presión de vapor del agua es 760 torr a 100°C, su punto de ebullición normal[3].
Tal vez hayan escuchado alguna vez, que a mayor altura menor presión. Es decir, que si estamos por ejemplo en una montaña por encima del nivel del mar y hervimos agua en un recipiente es de esperar que hierva a menos de 100° y que gastáremos más carbón para la cocción de los alimentos. También es muy común utilizar en nuestras cocinas ollas de presión, ya que cocinan más rápido porque el agua hierve a una temperatura más alta a altas presiones.
Ahora bien, cuando un líquido se caliente su presión de vapor aumenta, y si la temperatura es lo suficientemente alta se comienzan a formar burbujas de vapor debajo de la superficie, las cuales suben y estallan, lanzando así vapor al aire. En caso de que la presión de vapor de las burbujas sea menor a que la aplicada en la superficie del líquido, se rompen y no se produce así la ebullición.

Figura 2 . Ebullición del agua. Fuente: @yusvelasquez
¿Qué le sucede a la temperatura de ebullición del solvente puro al adicionar un soluto no volátil?
Cuando se adiciona un soluto no volátil a un disolvente puro, su presión de vapor disminuye, por ello la solución debe calentarse a una temperatura mayor que la del disolvente para que su presión de vapor sea igual a la presión atmosférica. Bajo estos fundamentos se basa la propiedad coligativa del aumento del punto de ebullición.
Matemáticamente se puede expresar según la Ley de Raoult, que establece que la elevación del punto de ebullición de un disolvente puro causada por la presencia de un soluto no volátil es proporcional al número de moles de soluto disuelto en un peso dado de disolvente.
Por tanto, se expresa como[2]:
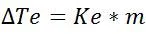
Aquí, el término ∆Te se refiere al aumento del punto de ebullición del disolvente, el cual viene dado por la diferencia del punto de ebullición de la solución menos el del disolvente puro, m es la molalidad de la solución y Ke es una constante denominada constante molal de elevación del punto de ebullición y que varía según el solvente, no depende del tipo de soluto.
A continuación les muestro el valor de algunas constantes para distintos disolventes
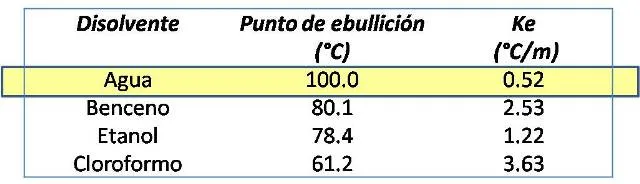
Datos tomados de Brown, T.[3]
A nivel de laboratorio se puede emplear el siguiente procedimiento experimental para la determinación de la masa molar, en este caso utilizando la urea como soluto no volátil.
PROCEDIMIENTO EXPERIMENTAL
Materiales y equipos:
- Vaso precipitado
- Cilindro graduado
- Termómetro
- Balón aforado
- Agitador de vidrio
- Perlas de ebullición
- Balanza
- Plancha de calentamiento
Dato teórico:
Podemos calcular teóricamente la masa molar de la urea y así compararla con el resultado.
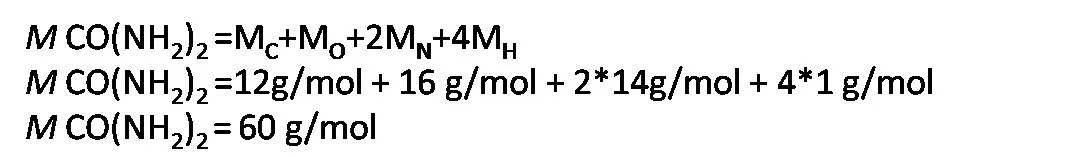
Pasos del procedimiento:
En primer lugar, se procede a determinar del punto de ebullición normal del solvente puro (Tºeb) para ello:
- Medimos 25 mL de agua destilada, en un cilindro graduado
- Posteriormente se trasvasan a un vaso precipitado de 50 mL.
- Se colocan algunas perlas de ebullición en el vaso precipitado, esto con la finalidad de que se produzca una ebullición homogénea.
- Se registra con el termómetro la temperatura inicial del solvente puro.

Figura 3. Medición de la temperatura inicial del solvente puro. Fuente:@yusvelasquez
Se calienta en la plancha hasta ebullición y se registra la temperatura Tºeb.(temperatura de ebullición del solvente puro)
Luego de ebullir, se registra la temperatura cada minuto hasta que permanezca constante, por un lapso de 3 – 5 minutos y se toma como la temperatura normal del solvente.

Figura 4. Temperatura de ebullición del solvente puro. Fuente @yusvelasquez
Como segundo paso, se procede a la determinación del punto de ebullición normal de la solución. (Teb) para ello:Pesamos en la balanza analítica 3 gramos de urea en un vaso precipitado.
Añadimos un poco de agua destilada, en vaso precipitado y removemos con el agitador de vidrio, para disolver el soluto.
Trasvasamos la solución preparada a un balón aforado de 25mL y se completa con agua destilada hasta el menisco. Tapar y agitar.

Figura 5: Preparación de la solución urea y agua. Fuente:@yusvelasquezTransvasamos la solución a un vaso precitado de 50 mL
Colocamos algunas perlas de ebullición en el vaso precipitado, para que se produzca una ebullición homogénea.

Figura 6. Calentamiento de la solución hasta ebullición. Fuente:@yusvelasquezRegistramos con el termómetro la temperatura inicial de la solución.
En una plancha calentamos la solución hasta ebullición y registramos la temperatura.
Finalmente, registramos después de ebullir la temperatura cada minuto, hasta que permanezca constante, por un lapso de 3 – 5 minutos. Se toma como la temperatura de ebullición de la solución.
A continuación se presentan los datos experimentales obtenidos en la experiencia práctica y que nos permitirán calcular la masa molar del compuesto estudiado.
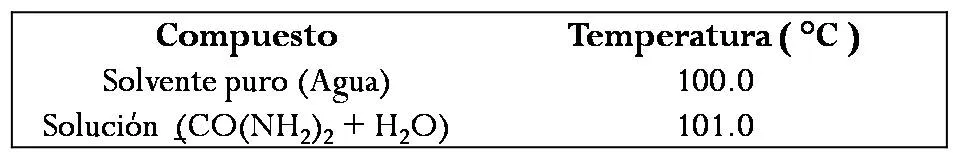
Cálculos
Para la determinación de la masa molar de la urea las ecuaciones empleadas son:

Como vemos al aplicar la propiedad coligativa del punto de ebullición en la determinación de la masa molar de la urea se obtuvo un resultado muy preciso con bajo porcentaje de error, por lo que puede emplearse a nivel de laboratorio con alta confiabilidad empleando el método presentado.
¡Espero les sea útil la información presentada, hasta una próxima oportunidad!
Referencias
- Atkins, P. y Jones, L. (2006). Principios de Química. Los caminos del descubrimiento. Panamericana
- Whitten K y Gailey K. (1985). Química General). Interamericana
- Brown, T. y Lemay, H. Química. La ciencia central. Prentice Hall
- Ramírez, D., Velásquez, Y., Lugo, O., Ferreira, M. Prácticas de laboratorio. UNEFM.
